Reconocimiento antigénico y respuesta inmune innata en la tuberculosis bovina
La tuberculosis en ganado bovino es una zoonosis ocasionada fundamentalmente por Mycobacterium bovis, aunque se han descrito casos en esta especie animal causados por M. tuberculosis y M. caprae. En general, nos referimos a la tuberculosis bovina como a la enfermedad causada por cualquiera de las especies incluidas dentro del complejo M. tuberculosis, y no exclusivamente a la originada por M. bovis. La respuesta inmune innata se produce en los animales tras la infección y previamente al desarrollo de una respuesta inmune adquirida. La relevancia de este tipo de respuesta viene dada por su capacidad para neutralizar el avance de la infección.
La principal ruta de entrada de la bacteria en el ganado bovino es aerógena, mediante inhalación (incluso con una carga bacteriana baja), y en menor medida por ingestión de organismos, pastos, agua o fómites contaminados. Otras rutas de infección posibles, aunque muy poco probables, son la vía venérea y la transmisión vertical. Diversos factores como la edad, el régimen de explotación o el clima pueden afectar a la probabilidad y modo de infección.
Por estudios desarrollados en animales de experimentación se ha observado que el tipo celular más importante en el primer contacto entre el sistema inmune innato del animal y la micobacteria es la célula fagocítica, que en el caso de una exposición vía aerógena es el macrófago alveolar, el cual a su vez forma parte del grupo de las células presentadoras de antígeno (APC). Estas células tratan de fagocitar la bacteria y de destruirla mediante la formación de fagolisosomas. La capacidad para eliminar la bacteria dependerá de factores relacionados con el sistema inmune del animal y de factores de virulencia propios de la bacteria. Como consecuencia de este proceso se puede provocar la destrucción de la micobacteria (en este punto la infección sería neutralizada y el animal no presentaría respuesta positiva en pruebas como la intradermotuberculinización) o bien puede conseguir sobrevivir, multiplicarse y generar la lisis del macrófago alveolar infectado. Cuando esto se produce acuden otras APC: células dendríticas y los monocitos, que volverán de nuevo a intentar la fagocitosis de la bacteria. Resulta paradójico que la APC sea una célula efectora clave en la destrucción de la micobacteria y que, al mismo tiempo, ésta sea la célula hospedadora preferida para su multiplicación.
Complejos estudios realizados con M. tuberculosis (y cuyos resultados pueden ser extrapolables a ganado bovino, al ser similar la ruta de entrada de la bacteria en ambas especies) han permitido comprender mejor el reconocimiento antigénico y la fagocitosis de la micobacteria, fenómenos paralelos, difíciles de resumir y que se realizan mediante diferentes receptores de las APC (Figura 1). En el reconocimiento inmune hay que destacar el protagonismo de los receptores tipo Toll o TLR (Toll-like receptors), un grupo de receptores filogenéticamente conservados e importantes mediadores de la inmunidad innata. En este sentido TLR-2 y TLR-4 en conjunción con CD14 (proteína de membrana) interactúan con componentes de la pared celular de la bacteria como lipoproteínas y lipoarabinomanano (LAM), componente fundamental de la pared las micobacterias. Otros menos estudiados, como el TLR-9, parecen intervenir en el reconocimiento del ADN bacteriano. De los TLR cabe destacar que no están sólo presentes en la superficie de la APC sino que también se encuentran en los fagosomas, por lo que el reconocimiento inmune se produce con o sin fagocitosis previa.
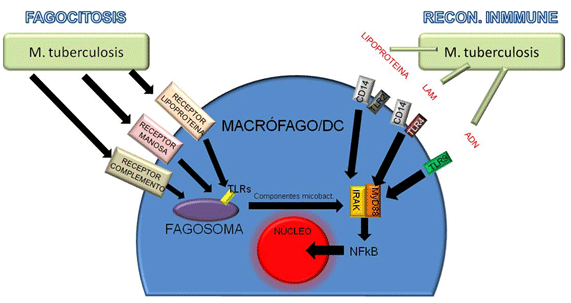
La micobacteria previamente opsonizada puede fijarse en la APC a través de receptores del complemento. Cuando la bacteria no está opsonizada, como es el caso en un primer contacto con el patógeno, el proceso es mediante receptores de la manosa, que reconocen manosa y fucosa en la superficie de la micobacteria, o por los denominados scavenger receptors, encargados de reconocer lipoproteínas de baja densidad. Los fagosomas formados, consecuencia del fenómeno de endocitosis, se fusionan posteriormente con lisosomas para constituir fagolisosomas. Los lisosomas son vacuolas que contienen potentes enzimas hidrolíticas cuya actividad óptima se desarrolla a pH ácido, condición que se da en el interior de los fagolisosomas (4.5-5) y que es mantenida gracias a una bomba de protones dependiente de ATP. La destrucción de la micobacteria en su interior conlleva la activación de una quinasa asociada al receptor de la interleuquina-1 (IL-1R-associated kinase-IRAK) que activa el factor de transcripción NF-Κb (factor nuclear kappa B) y provoca la liberación de diferentes citoquinas. Simultáneamente, a través de los TLR presentes en la membrana de la APC, se activa la proteína MyD88 (myeloid differentiation protein 88), que es el nexo de unión entre todos los TLR e IRAK y que es fundamental para la activación de las APC inducida por micobacterias. Hasta tal punto es importante la participación de los TLR funcionales de la membrana de las APC y los fagolisosomas que sin ellos (sólo mediante el fenómeno de fagocitosis) no se produciría la activación de las APC.
Citoquinas importantes en la respuesta frente a micobacterias
Citoquinas pro-inflamatorias:
La interacción entre la micobacteria y la célula fagocítica conlleva su activación y la producción de diversas citoquinas, lo cual su vez genera nuevas activaciones y producción de más citoquinas mediante complejos procesos de regulación. Esta producción de citoquinas juega un papel muy importante en la respuesta inflamatoria y en el desarrollo de la infección. Comentamos a continuación las más importantes:
-
Interferón gamma (IFN-γ): su papel protector es ampliamente conocido, principalmente en la respuesta específica por parte de las células T, y no tanto en la respuesta innata. Su producción in vitro en muestras de sangre previamente estimuladas con antígenos de micobacterias se utiliza como un marcador de infección. Los bovinos que son negativos a la prueba de intradermotuberculinización (IDTB) no producen IFN-γ específico frente al derivado proteico purificado (PPD) de M. bovis. Es interesante saber que la estimulación con PPD sólo provoca la producción de forma selectiva en los animales IDTB positivos mientras que en aquellos estimulados con un sonicado de la bacteria (producto obtenido tras sonicar, tratamiento aplicado con objeto de romper la pared bacteriana y que contiene, a diferencia de las PPD, componentes como poliglicanos y fosfolípidos) la producción de IFN-γ puede provocarse en animales IDTB positivos y negativos. En el caso de la producción inespecífica de IFN-γ el principal tipo celular involucrado son las células NK (natural killers). Otras células que se están estudiando como posibles productoras de IFN-γ en estas primeras fases son los macrófagos alveolares y las células T gamma-delta (Tγδ). Las células Tγδ contituyen en los bovinos (y en otros rumiantes) una gran proporción del total de las células mononucleares de sangre periférica.
-
Factor de necrosis tumoral alfa (TNF-α): su producción está inducida por la estimulación de monocitos, macrófagos y células dendríticas con micobacterias o sus productos. Tiene un papel fundamental en la formación de granulomas, activación macrofágica e inmunorregulación.
-
Interleuquina 1β (IL-1β): Producida por monocitos, macrófagos y células dendríticas. Se expresa en exceso en el lugar de infección y su carencia origina multiplicación bacteriana y alteraciones en la formación de los granulomas.
-
IL-6: posee propiedades pro y anti-inflamatorias. Por un lado se ha observado que puede inhibir la producción de TNF-α e IL-1β y por otro, su deficiencia aumenta la susceptibilidad a la infección debido a una deficiente producción de IFN-γ por parte del animal.
-
IL-12: es producida principalmente por células fagocíticas y se trata de una citoquina clave para inducir la producción de IFN-γ. La expresión de su receptor (IL-12R) está incrementada en los tejidos afectados.
-
IL-18 e IL-15: junto con IL-12 contribuyen a la producción de IFN-γ. IL-18 actúa en sinergia con IL-12 e IL-15 lo hace con otras citoquinas como IL-2, estimulando la activación y proliferación de células T y NK.
Citoquinas anti-inflamatorias:
Estas citoquinas se encargan de inhibir la producción o los efectos de las citoquinas pro-inflamatorias. Las más importantes son:
-
IL-10: producida por lo macrófagos tras la unión al LAM y fagocitosis de la bacteria (también puede ser producida por linfocitos T). IL-10 antagoniza la respuesta pro-inflamatoria mediante la disminución de la producción de IFN-γ, TNF-α e IL-12. En estudios realizados con individuos anérgicos con tuberculosis se ha observado que esta citoquina se encuentra en mayor proporción.
-
Factor de crecimiento transformante beta (TGF-β): esta citoquina, al igual que IL-10, es producida en exceso durante la tuberculosis por parte de monocitos y células dendríticas. Se la relaciona con el daño tisular y la fibrosis originada en la tuberculosis aunque sus actividades más destacables se engloban dentro de la respuesta inmune adquirida, ya que altera la presentación de antígeno y disminuye la producción de IFN-γ por parte de los linfocitos T.
-
IL-4: su acción se basa en suprimir la producción de IFN-γ y evitar la activación de los macrófagos. En infecciones experimentales se la ha relacionado con progresión de la enfermedad, reactivación de infecciones latentes e intensificación del daño tisular.
Quimioquinas importantes en la respuesta frente a micobacterias
Las citoquinas quimiotácticas o quimioquinas son las responsables del reclutamiento de células inflamatorias en el lugar de infección. Se conocen alrededor de 40 quimioquinas y 16 receptores de quimioquinas y algunas de ellas se han investigado en tuberculosis. Entre ellas destacamos:
• IL-8: producida por los macrófagos tras la fagocitosis. Atrae neutrófilos, linfocitos T y monocitos al lugar de infección.
• Proteína 1 quimiotáctica de monocitos: es producida por monocitos y macrófagos y actúa sobre ellos mismos (función autocrina). Su deficiencia provoca inhibición de la formación de granulomas.
• RANTES: es producida por una amplia variedad de células y se puede unir a múltiples receptores de quimioquinas. Su expresión en se relaciona con la formación de granulomas en pulmón.
Otros mecanismos de eliminación de micobacterias en la respuesta inmune innata
Existen otra serie de factores y células que pueden favorecer también la rápida eliminación de la bacteria antes del desarrollo de una respuesta inmune adquirida.
La vitamina D (1,25-dihidroxivitamina D) colabora con los macrófagos suprimiendo el crecimiento de M. tuberculosis. Existen estudios en humanos en los que su deficiencia se ha relacionado con una mayor susceptibilidad a la enfermedad.
Otro mecanismo de defensa es la producción de reactivos intermediarios del oxigeno (ROI) y del nitrógeno (RNI) en el interior de los macrófagos. A pesar de que algunas micobacterias se han mostrado resistentes a determinados ROI, los animales de experimentación con mutaciones específicas para su síntesis muestran mayor susceptibilidad a la infección. Respecto a los RNI, también se ha observado que una inhibición de iNOS (óxido nítrico sintasa) facilita la multiplicación bacteriana.
El gen Nramp1 codifica para la proteína de resistencia natural asociada a macrófagos (Nramp). Se trata de una proteína de membrana encargada del transporte iónico (principalmente Fe2+). El gen está involucrado en la activación del macrófagos y destrucción de micobacterias mediante la formación de radicales antimicrobianos en el interior del fagosoma.
El fenómeno de apoptosis también puede constituir un mecanismo innato de defensa frente a las micobacterias. La apoptosis de las células fagocíticas infectadas reduce la viabilidad de la bacteria intracelular, cosa que no se consigue mediante el proceso de necrosis. Esta apoptosis está inducida principalmente por TNF-α.
Neutrófilos, linfocitos T citotóxicos (Tc) y células NK son también tipos celulares que contribuyen a la eliminación de la micobacteria. Los gránulos de Tc y NK contienen granulisina, una molécula capaz alterar la membrana bacteriana.
Centro de Vigilancia Sanitaria Veterinaria (VISAVET)
Universidad Complutense
Bibliografía
Cvetnic, Z., V. Katalinic-Jankovic, B. Sostaric, S. Spicic, M. Obrovac, S. Marjanovic, M. Benic, B. K. Kirin, and I. Vickovic. 2007. Mycobacterium caprae in cattle and humans in Croatia. Int.J.Tuberc.Lung Dis. 11:652-658.
Flynn, J. L. and J. Chan. 2001. Immunology of tuberculosis. Annu.Rev.Immunol. 19:93-129.
Kennedy, H. E., M. D. Welsh, J. P. Cassidy, D. G. Bryson, F. Forster, J. McNair, B. Gangadharan, C. J. Howard, and J. M. Pollock. 2003. The role of WC1(+) gamma delta T-cells in the delayed-type hypersensitivity (DTH) skin-test reaction of Mycobacterium bovis-infected cattle. Vet.Immunol.Immunopathol. 93:169-176.
Pollock, J. M. and S. D. Neill. 2002. Mycobacterium bovis infection and tuberculosis in cattle. Vet.J 163:115-127.
Van Crevel, R., T. H. Ottenhoff, and J. W. van der Meer. 2002. Innate immunity to Mycobacterium tuberculosis. Clin.Microbiol.Rev. 15:294-309.


